SOLUCIONES ELECTROLITICAS
Soluciones electrolíticas
Se llaman soluciones electrolíticas a todas aquellas en las que el soluto se encuentra disuelto en el solvente formando iones.
En una solución de NaCl, KClo Na2SO4 no hay ni una sola molécula de cloruro de sodio, cloruro de potasio osulfato de sodio. Así:
NaCl ---------> Na+ + Cl-
KCl ----------> K+ + Cl-
Na2SO4 ---------> Na+ + Na+ + SO4-
Disociación electrolítica
Los iones, que están ya preformados en la sal, aun en su forma cristalina, se disocian al entrar en solución siempre y cuando haya alguna fuerza que pueda romper sus enlaces.
El sodio y el cloruro forman fácilmente una SAL, la de cloruro de sodio (NaCl), en la medida en que uno ha "cedido" 1 electrón y el otro lo ha "aceptado",convirtiéndose en los iones correspondientes.
El Cl- y el Na+ permanecerán unidos por atracción electroestática, formando un enlace iónico o electovalente. En el estado sólido, el NaCl forma un cristal, como muestra la Fig. 1. La estructura cristalina le ha hecho perder movilidad al ion Na+ y al ion Cl- y, en este estado, a pesar de haber iones positivos y negativos, el cloruro de sodio conduce muy mal la corriente eléctrica. Esto se debe a que no hay cargas eléctricas libres.
Si ahora, el NaCl es fundido o, más fácilmente, se disuelve en agua, los iones Na+ y Cl- , con sus cargas, quedan libres y la corriente eléctrica es conducida con mayor facilidad.
Este tipo de soluciones, formadas por iones y que conducen la corriente eléctrica son las llamadas soluciones electrolíticas.Caso contrario ocurre en las soluciones no electroliticas que son aquellas que no forman iones al disociarse y conducen poca electricidad.
Algunas de estas propiedades son función de lanaturaleza del soluto(color, sabor, densidad, viscosidad, conductividad eléctrica, etc.). Otras propiedades dependen del disolvente, aunque pueden ser modificadas por el soluto (tensión superficial, índice de refracción, viscosidad, etc.). Sin embargo, hay otras propiedades más universales que sólo dependen de la concentración del soluto y no de la naturaleza de sus moléculas. Estas son las llamadas propiedades coligativas.
DESCENSO DE LA PRESIÓN DE VAPOR
La presión de vapor de un disolvente desciende cuando se le añade un soluto no volátil. Este efecto es el resultado de dos factores:
-
la disminución del número de moléculas del disolvente en la superficie libre
-
la aparición de fuerzas atractivas entre las moléculas del soluto y las moléculas del disolvente, dificultando su paso a vapor
Cuanto más soluto añadimos, menor es la presión de vapor observada. La formulación matemática de este hecho viene expresada por la observación de Raoult de que el descenso relativo de la presión de vapor del disolvente en una disolución es proporcional a la fraccion molar del soluto.
Si representamos por P la presión de vapor del disolvente, P' la presión de vapor de la disolución y Xs la fracción molar del soluto, la ley de Raoult se expresa del siguiente modo:
de donde se obtiene que :
con lo que:
Esta fórmula nos permite enunciar la ley de Raoult: la presión de vapor de la disolución es igual a la presión de vapor del disolvente por la fracción molar del disolvente en la disolución. Esta fórmula tiene validez para todas las disoluciones verdaderas.
Cuando se trabaja con disoluciones diluidas como las biológicas, cuya molalidad oscila entre 0 y 0,4, se puede utilizar una fórmula aproximada. Si por ejemplo, la molalidad m = 0,4 hay 0,4 moles de soluto en 1000 g de agua, o lo que es lo mismo, 0,4 moles de soluto por cada 55,5 moles de agua, ya que 1000 g de agua (peso molecular =18) son 55,5 moles:
Por otro lado, la fracción molar del soluto (Xs) es:
y por lo tanto,
De acuerdo con esta fórmula, el descenso relativo de la presión de vapor es proporcional a la molalidad, si la disolución es diluída.
PUNTO DE EBULLICIÓN
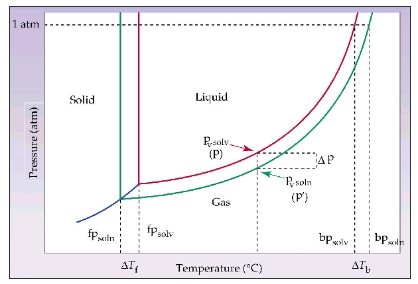
Cualquier disminución en la presión de vapor (como al añadir un soluto no volátil) producirá un aumento en la temperatura de ebullición (Ver Figura de la tabla). La elevación de la temperatura de ebullición es proporcional a la fracción molar del soluto. Este aumento en la temperatura de ebullición (DTe) es proporcional a la concentración molal del soluto:
DTe = Ke m
La constante ebulloscópica (Ke) es característica de cada disolvente (no depende de la naturaleza del soluto) y para el agua su valor es 0,52 ºC/mol/Kg. Esto significa que una disolución molal de cualquier soluto no volátil en agua manifiesta una elevación ebulloscópica de 0,52 º C.
DESCENSO CRIOSCÓPICO
La temperatura de congelación de las disoluciones es más baja que la temperatura de congelación del disolvente puro. La congelación se produce cuando la presión de vapor del líquido iguala a la presión de vapor del sólido. Llamando Tc al descenso crioscópico y m a la concentración molal del soluto, se cumple que:
DTc = Kc m
siendo Kc la constante crioscópica del disolvente. Para el agua, este valor es 1,86 ºC/mol/Kg. Esto significa que las disoluciones molales (m=1) de cualquier soluto en agua congelan a -1,86 º C.
PRESIÓN OSMÓTICA
La presión osmótica es la propiedad coligativa más importante por sus aplicaciones biológicas, pero antes de entrar de lleno en el estudio de esta propiedad es necesario revisar los conceptos de difusión y de ósmosis.
Difusión es el proceso mediante el cual las moléculas del soluto tienen a alcanzar una distribución homogénea en todo el espacio que les es accesible, lo que se alcanza al cabo de cierto tiempo (Figura de la izquierda). En Biología es especialmente importante el fenómeno de difusión a través de membranas, ya que la presencia de las membranas biológicas condiciona el paso de disolvente y solutos en las estructuras celulares (Figura de la derecha).
La presencia de una membrana separando dos medios diferentes impone ciertas restricciones al proceso de difusión de solutos, que dependerán fundamentalmente de la relación entre el diámetro de los poros de la membrana y el tamaño de las partículas disueltas. Las membranas se clasifican en cuatro grupos :
-
impermeables: no son atravesadas ni por solutos ni por el disolvente
-
semipermeables: no permiten el paso de solutos verdaderos, pero sí del agua
-
dialíticas: son permeables al agua y solutos verdaderos, pero no a los solutos coloidales
-
permeables: permiten el paso del disolvente y de solutos coloidales y verdaderos.
impermeables
semipermeables
Al hablar de disolvente nos referimos al agua, pero los solutos pueden ser:
-
coloidales (proteínas, polisacáridos)
-
verdaderos de tipo molecular (glucosa, urea)
-
verdaderos de tipo salino (NaCl, KHCO3)
Tomado de http://soluciones-elizabeth.blogspot.com.co/2011/10/soluciones-electroliticas.html